Besoin d'aide pour choisir le bon produit ?
Notre outil vous permettra de trouver le produit le mieux adapté à vos besoins.
Accéder au sélecteur de produitsBienvenue sur le site French
Nous avons détecté que vous préférez peut-être le site Global. Veuillez utiliser le menu déroulant ci-dessus pour modifier votre sélection si nécessaire.
La question de la surveillance des environnements de production et de stockage prend une place de plus en plus prépondérante au sein de l’Industrie pharmaceutique. La FDA et d’autres organismes de réglementation exigent non seulement des paramètres d’environnements ambiants de mesure et stockage précis, mais également l’utilisation de méthodes conformes à la réglementation 21 CFR Part 11, si le support de stockage est électronique.
La surveillance en matière de stabilité des produits médicaux est également assujettie aux normes dressées par l’ICH (International Conference on Harmonization of Technical Requirements for Registration of Pharmaceuticals for Human Use, ou Conférence internationale sur l’harmonisation des exigences techniques pour l’enregistrement des produits pharmaceutiques à usage humain) et aux lignes directives finales de l’ICH (validées en février 2003) ; ces normes de surveillance sont désormais appliquées à travers toute l’Europe, au Japon et aux Etats-Unis.
La FDA stipule également, dans le cadre de la réglementation 21 CFR Part 203, que les fabricants, les distributeurs autorisés de médicaments et leurs représentants peuvent conserver et manipuler tous les échantillons médicamenteux, à la condition express de converser la stabilité, l’intégrité et l’efficacité de ces dits échantillons et de veiller à ce qu’ils ne comportent aucune trace de contamination, détérioration, ni altération.
Outre les chambres d’environnement, peuvent être également contrôlés la température, le taux d’humidité, les numérations de particules, la pression différentielle, l’éclairage, les teneurs en gaz et d’autres conditions environnementales. Ces contrôles peuvent être étendus aux équipements requis pour détecter les gaz toxiques et les emplacements des hottes d’évacuation de fumées.
Les organismes de réglementation exigent que les installations de stabilité répondent aux critères suivants :
La mesure et l’enregistrement des températures sont primordiales en matière de stockage des données périssables, mais l’enregistrement d’une moyenne peut se faire de plusieurs façons.
D’après la définition de la ICH, la température cinétique moyenne est « l’image du stress thermique d’un composant du médicament ou du médicament lui-même qui aurait subi des variations de température hautes et basses, durant une période définie ».
La MKT exprime la tension thermique cumulée à laquelle a été exposé un produit à des températures changeantes, pendant les phases de stockage et de distribution. Elle diffère des autres moyennes (comme la moyenne numérique unique ou la moyenne arithmétique) dans la mesure où il est accordé plus de crédit aux températures les plus élevées pour calculer la moyenne, reconnaissant de la sorte l’accélération de la dégradation thermique des matériaux à des températures plus élevées.

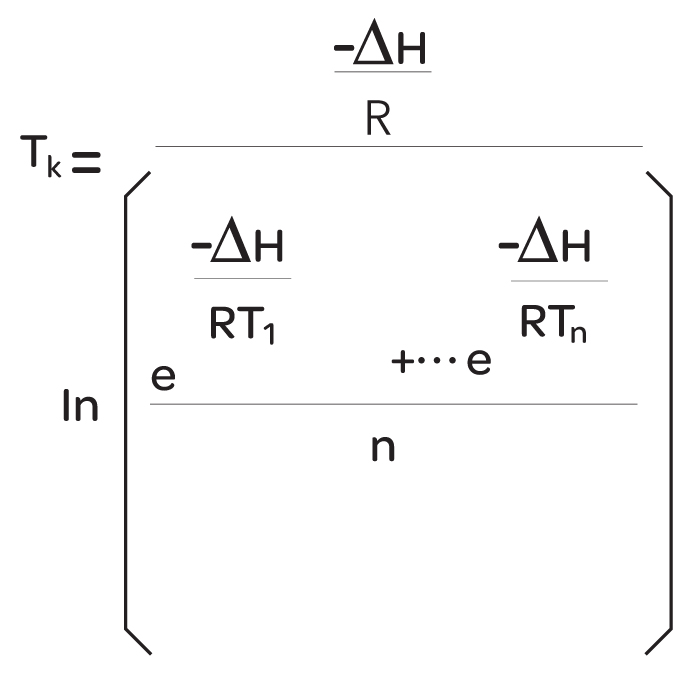
La température de la moyenne cinétique est calculée comme étant :
La TK instaurée comme température cinétique moyenne est donnée en Kelvin
ÄH correspond à l’activation de chaleur en kJoule par mole
R correspond à la constante universelle en gaz en kJoule par mole par Kelvin
T1 et Tn sont les échantillons de température pour les périodes 1 et n, respectivement
n correspond au nombre total de périodes inclus dans le calcul
Il existe tout un nombre d’interprétations sur la manière dont ce calcul est réalisé à l’aide d’échantillons réels :
Eurotherm propose toutes les méthodes énoncées ci-dessus avec :
La détection et la signalisation de conditions anormales représentent un des éléments clés des systèmes de surveillance environnementale.
Les entreprises pharmaceutiques doivent adopter tout un panel de méthodes pour capter et signaler toutes les conditions considérées comme anormales. Ces méthodes doivent permettre entre autres de :
Sélecteur de produits
Notre outil vous permettra de trouver le produit le mieux adapté à vos besoins.
Accéder au sélecteur de produitsNous contacter