Hai bisogno di aiuto per scegliere il prodotto giusto?
Il nostro strumento ti aiuterà a trovare il prodotto più adatto alle tue esigenze
Accedi allo strumento di selezione dei prodottiBenvenuto sul sito Italiano
Abbiamo rilevato che potresti preferire il sito Global. Se necessario, utilizza il menu a tendina delle lingue per modificare la scelta.
Nel settore farmaceutico, la conformità nei confronti delle specifiche Alcoa permette di innalzare i livelli di qualità e sicurezza dei dati, del prodotto e dei processi produttivi. Questo articolo descrive i requisiti concettuali di Alcoa(+), i problemi che puntano a risolvere e alcune delle soluzioni di acquisizione dati disponibili per aiutare a rispettare le linee guida.
di Sébastien Girard, Eurotherm by Schneider Electric

Il futuro dell’automazione nelle scienze della vita è legato a doppio filo all’industria 4.0, si sente sempre più spesso citare il concetto di Pharma 4.0, tecnologie come intelligenza artificiale, machine learning, cloud computing, IIOT, analisi avanzata dei dati, realtà aumentata, digital twin e altre ancora, saranno sempre più presenti in questo settore, ma tutte dovranno essere conformi alle normative e alle linee guida delle organizzazioni governative. Un aspetto sul quale enti consultivi e regolatori hanno concordato è il concetto Alcoa(+), relativo all’integrità dei dati. Agenzia Europea per i Medicinali (EMA), FDA (Food and Drug Admnistration per gli USA) e ISPE (International Society for Pharmaceutical Engineering) hanno già pubblicato alcuni documenti di orientamento sull’argomento e il PIC/S (Pharmaceutical Inspection Convention and Pharmaceutical Inspection Co-operation Scheme) ha pubblicato una bozza di documento. Di recente l’Organizzazione mondiale della sanità (OMS) ha anche presentato una bozza di commenti che sta circolando tra esperti e organizzazioni per la revisione. In qualità di fornitore di automazione esperto e affermato nel settore, Eurotherm by Schneider Electric fa parte di tale processo di revisione.
ALCOA è un quadro di riferimento, introdotto all’inizio degli anni ’90 dalla FDA, che definisce un insieme di principi a salvaguardia dell’integrità dei dati. Si tratta di un acronimo, secondo il quale i dati devono essere: Attribuibili, Leggibili, Contemporanei, Originali e Accurati. Il concetto di ALCOA è stato esteso negli anni ad ALCOA+ che richiede che i dati siano anche Completi, Coerenti, Duraturi e Disponibili per il loro intero Ciclo di Vita.
Sul mercato sono disponibili molte soluzioni di acquisizione e gestione dei dati, è importante saper riconoscere i rischi aziendali che si corrono in presenza di sistemi di gestione dei dati mal progettati e quindi in mancanza di integrità dei dati. Comprendere il motivo per cui ALCOA+ è stato introdotto e capirne i requisiti aiuterà gli interessati a scegliere il fornitore giusto e ad investire nella soluzione più efficace.
Quindi, quali sono i requisiti ALCOA nel dettaglio, quali problemi stanno cercando di risolvere e quali soluzioni sono disponibili?
Attribuibili
In primo luogo, i dati devono essere collegabili alla loro fonte, quindi attribuibili all’individuo o al sistema che li ha osservati e registrati, nonché riferibili alla fonte dei dati stessi. Le modifiche apportate ai dati devono essere firmate e datate dalla persona che effettua le modifiche. Talvolta la necessità di contenere i costi delle licenze e la lentezza dei dipartimenti IT nella creazione di account utente favoriscono la cattiva pratica di condividere un’unica password tra più operatori. In una situazione di questo tipo gli addetti possono apportare modifiche non univocamente attribuibili, l’integrità dei dati viene quindi meno. Il concetto di Attribuibilità si applica non solo alla raccolta di dati originali, ma anche alle eventuali modifiche apportate durante l’analisi e il reporting.
Le soluzioni di acquisizione dei dati spaziano dal singolo registratore videografico al sistema di gestione dei dati progettato a livello di impianto. Nello scegliere una soluzione è essenziale individuare prodotti e sistemi con funzioni di gestione degli utenti e audit trail che consentano di disporre di account protetti da password individuali e in grado di richiedere l’autorizzazione per attività specifiche, in funzione del ruolo. Come parte dell’audit trail, le modifiche di input di dati a parametri di controllo, setpoint, riconoscimento di allarmi e azioni simili dovrebbero essere automaticamente registrate con un timestamp (indicazione di data e ora). Può anche rivelarsi utile una funzione di gestione della sicurezza collegabile a Microsoft® Active Directory, per semplificare e centralizzare la gestione degli utenti.
Leggibili
I dati raccolti devono essere una registrazione chiara e permanente, leggibile o interpretabile in qualsiasi momento, durante il periodo di conservazione. Esempi di documenti poco leggibili sono quelli scritti a mano con calligrafia poco chiara, quelli stampati su carta per stampanti termiche e ormai sbiaditi, quelli che riportano un ridimensionamento inadeguato di intervalli di dati e audit trail complessi. Se i dati non possono essere letti correttamente, vengono introdotti rischi durante la revisione dei dati ai fini di analisi della qualità e di controllo.
Passare da registratori a carta con report cartacei manuali a registratori videografici e software di reporting consente di ridurre le registrazioni redatte a mano. I dati registrati digitalmente possono quindi essere archiviati, recuperati e stampati, fornendo un audit trail leggibile per la revisione periodica. In genere, i file di dati registrati possono essere archiviati e rivisti utilizzando un pacchetto software. Utilizzare un software in grado di cercare automaticamente i dati in base al nome del dispositivo di registrazione, al gruppo, al codice del lotto o all’intervallo di date, rende più semplice e rapido il recupero dei dati. Alcuni registratori videografici includono l’opzione Auditor che consente di aggiungere commenti, nonché l’approvazione o la convalida mediante firme elettroniche in qualsiasi momento durante l’analisi. È importante che queste note vengano archiviate insieme ai dati originali in modo che possano essere facilmente recuperate quando necessario. Scegliere un software in grado di stampare automaticamente grafici, valori di canale, messaggi e allarmi al completamento del batch risulta particolarmente utile per gli addetti alla funzione qualità all’interno dell’azienda. Per poter analizzare e creare report è inoltre utile che i dati siano archiviati in un server storico; esistono soluzioni che prevedono pacchetti di report digitali per la creazione di report più o meno sofisticati, creati manualmente o automaticamente sulla base di modelli definiti.
Contemporanei
I dati devono essere registrati nel momento in cui sono stati generati o il più vicino possibile all’evento osservato. La retrodatazione dei dati può infatti comportare errori e le informazioni possono essere parzialmente o completamente dimenticate se riportate al termine della giornata o del processo. Un altro esempio di cattiva pratica è il riutilizzo dei precedenti risultati batch validi o il riesame di risultati borderline che possono falsificare il vero stato di superamento/fallimento di uno specifico lotto. Pertanto, i requisiti richiedono il timestamp senza intervento manuale, con gli orologi di strumenti e computer sincronizzati con il sistema, in genere tramite un server SNTP (Simple Network Time Protocol).
Anche in questo caso l’utilizzo di dispositivi di registrazione digitali consente di inserire e registrare i commenti associati al riconoscimento di allarmi o alle modifiche dei parametri firmati nel momento in cui si verifica l’evento. La raccolta di dati di processo e di allarme dovrebbe essere automatica, tramite funzioni predeterminate e validate, senza intervento manuale. I commenti di riconoscimento degli allarmi e le firme di modifica dei parametri devono essere inseriti automaticamente, in corrispondenza del relativo timestamp. Per la sincronizzazione automatica dell’ora è opportuno scegliere dispositivi che possono essere collegati in rete a un server SNTP. Alcuni registratori videografici sono disponibili con funzionalità server SNTP integrata, per la sincronizzazione dei dispositivi collegati.
Originali
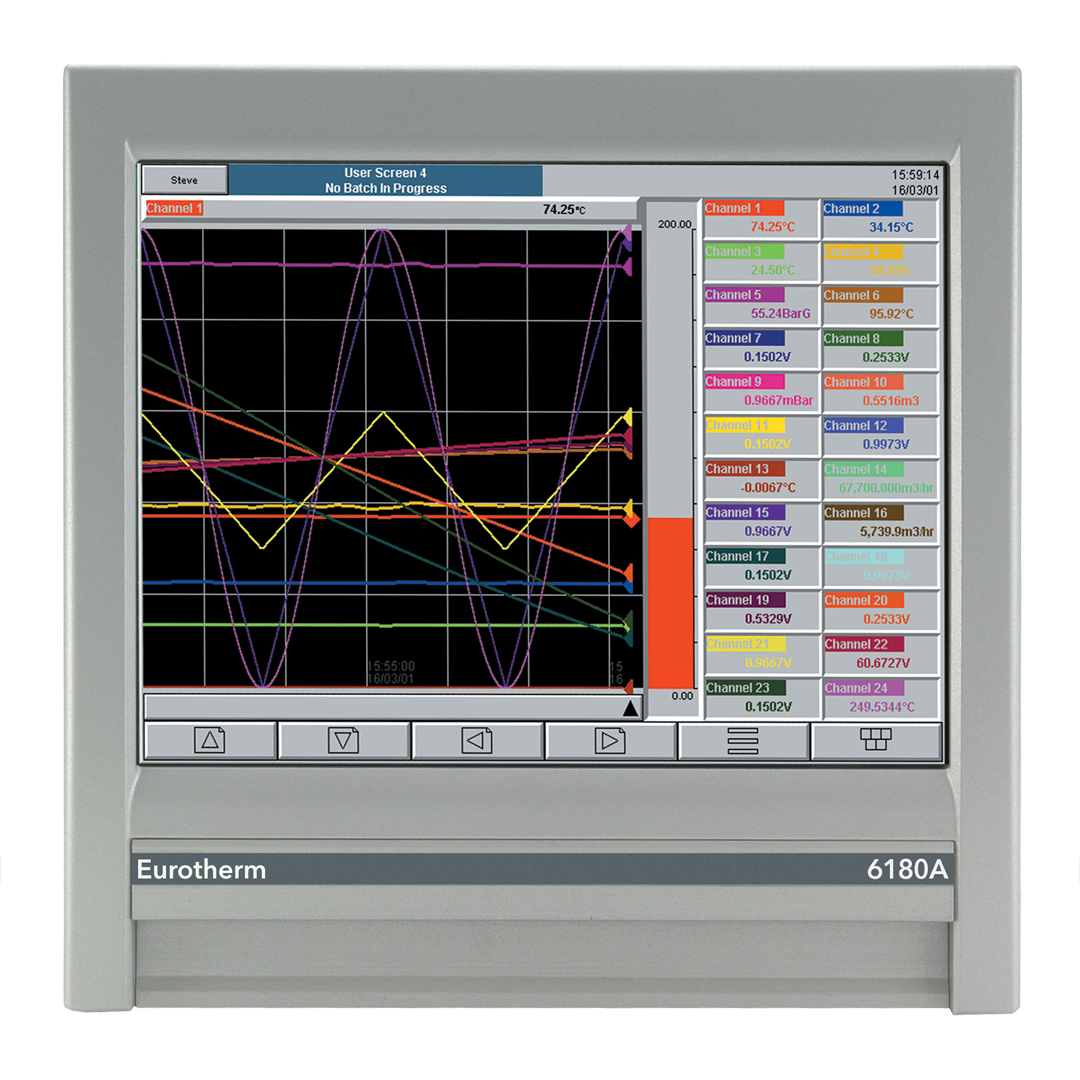
I dati originali, definiti come “fonte” o “dati grezzi”, sono generalmente considerati il primo record e quindi il più accurato e affidabile. Che si tratti di un risultato negativo o positivo (pass/fail), questi dati devono essere conservati nel loro stato originale inalterato o registrati come copia autentica per riferimento. Eventuali calcoli, report e risultati di analisi sono considerati “metadati” rispetto ai dati non elaborati. Durante i controlli, i revisori si aspettano di essere in grado di ricondurre i metadati, come ad esempio i report, direttamente ai dati sorgente/non elaborati. Poiché i dati possono essere facilmente modificati e interpretati in modo errato, l’uso di record cartacei può essere fonte di problemi: la riscrittura dei dati può comportare errori nella trascrizione, l’arrotondamento inadeguato dei valori numerici può portare a risultati falsati e così via. Per quanto riguarda invece i record digitali la registrazione dei dati nel formato di file .CSV, comunemente usato per rappresentare i dati originali, essendo un formato facilmente modificabile, non può considerarsi affidabile.
Per aiutare le aziende farmaceutiche a dimostrare la validità dei loro dati originali alcuni fornitori di apparecchiature hanno sviluppato i propri formati di file proprietari antimanomissione. Ad esempio, nei registratori di dati Eurotherm come il registratore/regolatore nanodac™, il registratore videografico serie 6000, il registratore modulare versadac™ e il PAC T2750, i dati di processo e i messaggi di allarme sono memorizzati in un formato di file UHH a controllo binario. Tendenze e report possono essere letti da questo formato di file utilizzando lo strumento software proprietario Data Reviewer che utilizza funzioni predeterminate e può essere convalidato per la creazione di una copia vera. Questo software è anche in grado di individuare e rifiutare i record modificati.
Accurati
La precisione è un elemento implicito della qualità dei dati nelle linee guida GxP. I set di dati dovrebbero riflettere correttamente l’azione o l’osservazione effettuata e i dati dovrebbero essere controllati ove necessario. Eventuali modifiche devono essere spiegate, se non immediatamente evidenti. Gli esperti sono ormai concordi nell’incoraggiare la registrazione elettronica dei dati in luogo di quella su carta, oltre a suggerire l’integrazione di controlli di precisione nella progettazione del sistema elettronico. È necessario prestare attenzione quando si sceglie una soluzione di registrazione: il dispositivo di registrazione deve avere adeguati livelli di precisione. Anche il posizionamento dei sensori merita attenzione, una loro errata collocazione potrebbe infatti generare letture sbagliate o non accurate. Non bisogna poi sottovalutare le tarature degli strumenti, che devono essere eseguite a intervalli specifici, al fine di stabilire la precisione dei dispositivi utilizzati.
Il formato elettronico può offrire una maggior precisione dei dati e una risoluzione più elevata rispetto ai record cartacei. Nello scegliere una soluzione di acquisizione dati è opportuno porre particolare attenzione alle caratteristiche degli ingressi che devono essere ad alta precisione e progettati per fornire misurazioni precise anche in ambienti di produzione elettricamente rumorosi. Solitamente, nei registratori videografici, l’impostazione del range dei parametri per l’immissione di limiti di dati è piuttosto semplice. Le procedure per la taratura del loop dello strumento sono utili per confermare i valori letti siano rappresentativi delle condizioni di processo effettive. Esistono aziende che offrono servizi di taratura completi, tra queste, quelle specializzate in applicazioni farmaceutiche offrono anche servizi di convalida secondo le linee guida ISPE Gamp®5.
Completi, Coerenti, Duraturi, Disponibili, per l’interno Ciclo di Vita
I dati devono essere Completi: devono essere raccolti tutti i dati grezzi e i metadati rilevanti, inclusi i test e le rianalisi. Per Coerenza, tutti gli elementi dell’analisi devono riportare data e ora ed essere nella sequenza prevista, comprese le deviazioni verificatesi durante il processo e qualsiasi modifica apportata ai dati. I record di dati devono essere Duraturi e quindi archiviati e conservati come documenti o su supporti elettronici e devono essere Disponibili e leggibili dal personale responsabile per la revisione, l’audit o l’ispezione in qualsiasi momento durante il periodo di conservazione richiesto. I principi ALCOA+ si applicano in tutte le fasi del ciclo di vita dei dati, dall’iniziale generazione e registrazione attraverso l’elaborazione, l’uso, la conservazione dei dati, l’archiviazione e il recupero fino alla data di distruzione.
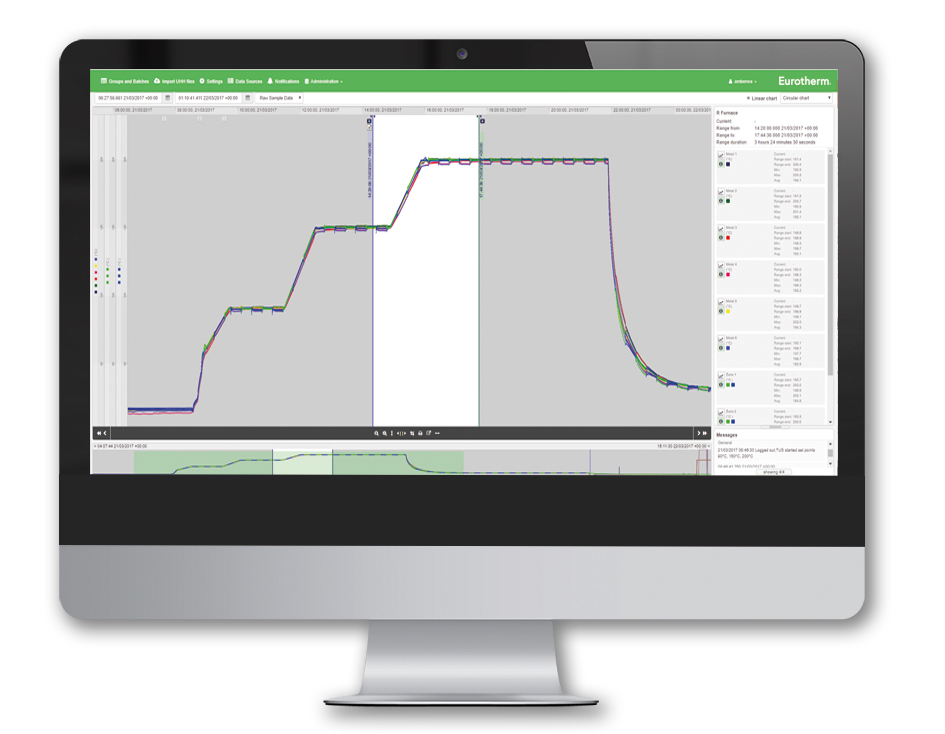
Per facilitare l’acquisizione di dati completi è utile scegliere soluzioni in grado di memorizzare nello stesso file di dati tutte le informazioni rilevanti come valori di processo, dettagli del batch, cronologia degli allarmi e audit trail. Le funzionalità progettate per le attività di audit dovrebbero essere in grado di acquisire informazioni come modifiche di allarme e commenti di riconoscimento per la revisione. Utilizzare registratori videografici con memoria integrata consente la registrazione dei dati nel momento corretto e al punto di misura, inoltre la possibilità di memorizzare i dati direttamente nel dispositivo di registrazione riduce il rischio di perdita degli stessi in caso di interruzione temporanea della comunicazione: i dati registrati localmente possono infatti essere utilizzati per colmare l’intervallo “vuoto” nel database remoto, successivamente al ripristino della comunicazione. Rimane sempre valido il fatto che i dati devono essere archiviati con indicazione di data e ora (timestamp) per favorirne la coerenza, mentre i formati di file elettronici a prova di manomissione e l’uso di data historian ad alta integrità consentono l’archiviazione a lungo termine e la disponibilità dei dati per tutta la vita del record (generalmente si tratta di una data successiva alla data di scadenza del prodotto farmaceutico). In applicazioni critiche è possibile, oltre che opportuno, implementare un’architettura di sistema ad alta disponibilità, inclusi gruppi di continuità (UPS) e strumentazione ridondante, server, historian e reti di di comunicazione.
Nel mio ruolo di Global Business Development Manager di Eurotherm per il segmento Consumer Packaged Goods, viaggio spesso e incontro clienti in tutto il mondo, fino a poco tempo fa molte aziende dell’aera Asia-Pacifico, ad esempio in India o in Cina, non erano orientate a seguire le linee guida ALCOA+ per l’integrità dei dati. In parte perché a livello nazionale non era obbligatorio e, non esportando negli Stati Uniti o in Europa, non avevano una stringente necessità di conformarsi, ma anche perché adeguarsi a questi principi implica investimenti in attrezzature e in formazione del personale con un inevitabile impatto sulla redditività e quindi sulla competitività sul mercato. La situazione sta però cambiando e in un futuro molto prossimo non avranno alcuna opzione, perché le linee guida dell’OMS allineeranno i produttori a livello globale, a tutto vantaggio dei pazienti che ricevono assistenza sanitaria in tutto il mondo.
Questo periodo di allineamento delle linee guida a livello mondiale rappresenta senza dubbio il momento giusto per investire in nuove tecnologie Pharma 4.0 e adattare i sistemi di gestione della qualità e i processi di produzione esistenti per innalzare i livelli di qualità del prodotto e di sicurezza per i pazienti. Tutti hanno diritto ad accedere a medicinali sicuri e questo è il momento giusto per ottenere la fiducia dei consumatori ed essere credibili ai loro occhi. Le industrie farmaceutiche hanno necessità di valutare nuovi processi produttivi, come la produzione single-use o quella continua, invece del tradizionale concetto di produzione in lotti. L’acquisizione e la protezione dei dati dovranno essere integrate nel cuore del processo di produzione e dovrebbero essere incluse nella fase di progettazione del sistema di produzione come parte di un approccio di sviluppo sistematico noto come Quality by Design (QbD). Questo approccio deve essere applicato all’intero ciclo di vita della gestione dei dati, dall’acquisizione fisica dei parametri fino all’automazione, alla reportistica della tracciabilità, alla memorizzazione, all’analisi, all’archiviazione e alla distruzione dei dati. Non ha senso implementare una strategia di alto livello per migliorare l’efficienza o per incrementare la qualità del prodotto, se non si considerano le conseguenze legate alla presenza di dati errati o modificati (non integri) ad esempio, in un nuovo algoritmo di controllo all’interno di un sistema di intelligenza artificiale o in un sistema di calcolo analitico. La paura di un audit non dovrebbe più essere il fattore decisivo nel convincere i produttori a dotarsi di un buon programma di gestione dell’integrità dei dati. Piuttosto, la fiducia in dati affidabili in grado di aiutare a rendere più efficiente la produzione, al livello di qualità richiesto, dovrebbe essere il fattore di business decisivo.
Le soluzioni per l’acquisizione di dati ad alta integrità possono essere facilmente integrate in piattaforme Industry 4.0, IioT, basate su cloud, le aziende farmaceutiche possono così godere di dati, conformi alle linee guida ALCOA+, da utilizzare nelle tecnologie intelligenti di prossima generazione.
Questo articolo è apparso sul numero di Aprile 2020 della Rivista Automazione e Strumentazione.
L’autore è Sébastien Girard, Global Business Development Manager Consumer Packaged Goods di Eurotherm by Schneider Electric.
Strumento di selezione dei prodotti
Il nostro strumento ti aiuterà a trovare il prodotto più adatto alle tue esigenze
Accedi allo strumento di selezione dei prodottiContattaci